Белки, их строение и функции. Урок «Белки – природные биополимеры Краткая характеристика физических, физико-химических и химических свойств белка
Среди органических веществ белки , или протеины , - самые многочисленные, наиболее разнообразные и имеющие первостепенное значение биополимеры. На их долю приходится 50 - 80% сухой массы клетки.
Молекулы белков имеют большие размеры, поэтому их называют макромолекулами . Кроме углерода , кислорода , водорода и азота , в состав белков могут входить сера, фосфор и железо. Белки отличаются друг от друга числом (от ста до нескольких тысяч), составом и последовательностью мономеров. Мономерами белков являются аминокислоты (рис. 1)
Бесконечное разнообразие белков создается за счет различного сочетания всего 20 аминокислот. Каждая аминокислота имеет свое название, особое строение и свойства. Их общую формулу можно представить в следующем виде:
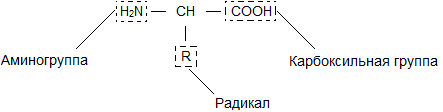
Молекула аминокислоты состоит из двух одинаковых для всех аминокислот частей, одна из которых является аминогруппой (-NH 2 ) с основными свойствами, другая - карбоксильной группой (-COOH ) с кислотными свойствами. Часть молекулы, называемая радикалом (R ), у разных аминокислот имеет различное строение. Наличие в одной молекуле аминокислоты основной и кислотной групп обусловливает их высокую реакционную способность. через эти группы происходит соединение аминокислот при образовании белка. При этом возникает молекула воды, а освободившиеся электроны образуют пептидную связь. Поэтому белки называют полипептидами .
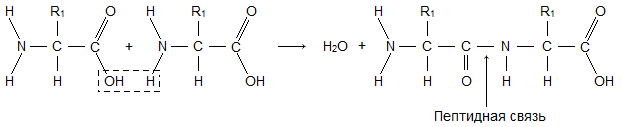
Молекулы белков могут иметь различные пространственные конфигурации, и в их строении различают четыре уровня структурной организации.
Последовательность аминокислот в составе полипептидной цепи представляет первичную структуру
белка. Она уникальна для любого белка и определяет его форму, свойства и функции.
Большинство белков имеют вид спирали в результате образования водородных связей между -CO-
и -NH-
группами разных аминокислотных остатков полипептидной цепи. Водородные связи малопрочные, но в комплексе они обеспечивают довольно прочную структуру. Эта спираль - вторичная структура
белка.
Третичная структура - трехмерная пространственная «упаковка» полипептидной цепи. В результате возникает причудливая, но для каждого белка специфическая конфигурация - глобула . Прочность третичной структуры обеспечивается разнообразными связями, возникающими между радикалами аминокислот.
Четвертичная структура
характерна не для всех белков. Она возникает в результате соединения нескольких макромолекул с третичной структурой в сложный комплекс. Например, гемоглобин крови человека представляет комплекс из четырех макромолекул белка.
Такая сложность структуры белковых молекул связана с разнообразием функций, свойственных этим биополимерам.
Нарушение природной структуры белка называют денатурацией
. Она может происходить под воздействием температуры, химических веществ, лучистой энергии и других факторов. При слабом воздействии распадается только четвертичная структура, при более сильном - третичная, а затем - вторичная, и белок остается в виде полипептидной цепи.
Этот процесс частично обратим: если не нарушена первичная структура, то денатурированный белок способен восстанавливать свою структуру. Отсюда следует, что все особенность строение макромолекулы белка определяются его первичной структурой.
Кроме простых белков , состоящих только из аминокислот, есть еще и сложные белки
Отправить свою хорошую работу в базу знаний просто. Используйте форму, расположенную ниже
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Размещено на http://www.сайт/
1. Болезни, обусловленные нарушением синтеза функционирования белков
Белки являются теми химическими соединениями, деятельность которых ведет к формированию нормальных признаков здорового организма. Прекращение синтеза того или иного белка или изменение его структуры ведет к формированию патологических признаков и развитию болезней. Назовем несколько заболеваний, обусловленных нарушением структуры или интенсивности синтеза белков.
Классическая гемофилия обусловлена отсутствием в плазме крови одного из белков, участвующих в свертывании крови; у больных людей наблюдается повышенная кровоточивость
Серповидноклеточная анемия обусловлена изменением первичной структуры гемоглобина: у больных людей эритроциты имеют серповидную форму, число эритроцитов уменьшено в результате ускоренного процесса их разрушения; гемоглобин связывает и переносит меньшее, чем в норме, количество кислорода.
Гигантизм обусловлен повышенным количеством гормона роста; больные имеют чрезмерно высокий рост.
Дальтонизм обусловлен отсутствием пигмента колбочек сетчатки, участвующем в формировании восприятия цвета; дальтоники не различают некоторые цвета.
Диабет связан с так называемой недостаточностью гормона инсулина, которая может быть обусловлена разными причинами: уменьшением количества или изменением строения выделяемого инсулина, уменьшением количества или изменением структуры рецептора инсулина. У больных людей наблюдается повышенное количество глюкозы в крови и развиваются сопутствующие этому патологические признаки.
Злокачественная холестеринемия обусловлена отсутствием в цитоплазматической мембране клеток нормального рецепторного белка, узнающего транспортный белок, переносящий молекулы холестерина; в организме больных нужный клеткам холестерин не проникает в клетки, а в больших количествах скапливается в крови, откладывается в стенке кровеносных сосудов, что ведет к их сужению и быстрому развитию гипертонии в раннем возрасте.
Прогрессирующая ксеродерма обусловлена нарушением работы ферментов, которые в норме осуществляют восстановление в клетках кожи участков ДНК, повреждающихся УФ-лучами; больные не могут находиться на свету, так как в этих условиях у них возникают многочисленные кожные язвы и воспаление.
8. Муковисцидоз обусловлен изменением первичной структуры белка, формирующего в наружной плазматической мембране канал для ионов СГ; у больных в воздухоносных путях скапливается большое количество слизи, что ведет к развитию заболеваний органов дыхания.
2. Протеомика
Ушедший XX век характеризовался возникновением и бурным развитием научных дисциплин, которые расчленяли биологическое явление на составляющие его компоненты и стремились объяснить явления жизни через описание свойств молекул, в первую очередь биополимеров, входящих в состав живых организмов. Этими науками были биохимия, биофизика, молекулярная биология, молекулярная генетика, вирусология, клеточная биология, биоорганическая химия. В настоящее время развиваются научные направления, которые пытаются, исходя из свойств составляющих, дать целостную картину всего биологического явления. Для этой новой, интегративной стратегии познания жизни требуется громадный объем дополнительной информации. Науки нового века - геномика, протеомика и биоинформатика уже начали поставлять для нее исходный материал.
Геномикабиологическая дисциплина, изучающая структуру и механизм функционирования генома в живых системах. Геном - совокупность всех генов и межгенных участков любого организма. Структурная геномика изучает строение генов и межгенных участков, играющих большое значение в регуляции активности генов. Функциональная геномика изучает функции генов, функции их белковых продуктов. Предметом изучения сравнительной геномики являются геномы разных организмов, сравнение которых позволит понять механизмы эволюции организмов, неизвестные функции генов. Геномика возникла в начале 90-х годов XX века вместе с проектом "Геном человека". Задача этого проекта состояла в том, чтобы определить последовательность всех нуклеотидов в геноме человека с точностью до 0,01%. К концу 1999 года полностью раскрыто строение генома многих десятков видов бактерий, дрожжей, круглого червя, дрозофилы, растения арабидопсиса. В 2003 году расшифрован геном человека. Геном человека содержит около 30 тысяч белок-кодирующих генов. Только для 42% из них известна их молекулярная функция. Оказалось, что с дефектами генов и хромосом связано лишь 2% всех наследственных заболеваний; 98% заболеваний связаны с нарушением регуляции нормального гена. Гены проявляют свою активность в синтезируемых белках, выполняющих в клетке и организме различные функции.
В каждой конкретной клетке в определенный момент времени функционирует определенный набор белков - протеом. Протеомика - наука, изучающая совокупность белков в клетках при разных физиологических состояниях и в разные периоды развития, а так же функции этих белков. Между геномикой и протеомикой есть существенная разница - геном стабилен для данного вида, тогда как протеом индивидуален не только для разных клеток одного организма, но и для одной клетки в зависимости от ее состояния (деление, покой, дифференцировка т.д.). Множество протеомов, свойственное многоклеточным организмам, создает огромную трудность их изучения. Пока даже неизвестно точное число белков в человеческом организме. По некоторым оценкам их сотни тысяч; лишь несколько тысяч белков уже выделены, еще меньшая их часть подробно изучена. Идентификация и описание белков - это чрезвычайно сложный технически процесс, требующий комбинации биологических и компьютерных методов анализа. Однако разрабатываемые в последние годы методы выявления продуктов активности генов - молекул и РНК и белков - позволяют надеяться на быстрый прогресс в этой области. Уже сейчас созданы методы, позволяющие одновременно выявлять сотни клеточных белков одновременно и сравнивать белковые наборы в разных клетках и тканях в норме и при разных патологиях. Одним из таких методов является использование биологических чипов, позволяющих обнаруживать в изучаемом объекте сразу тысячи разных веществ: нуклеиновых кислот и белков. Открываются большие возможности для практической медицины: имея протеомную карту, подробный атлас всего комплекса белков, врачи наконец получат долгожданную возможность лечить само заболевание, а не симптомы.
Геномика и протеомика оперирует с такими огромными массивами информации, что возникла острая потребность в биоинформатике - науке, которая собирает, сортирует, описывает, анализирует и перерабатывает новую информацию о генах и белках. Используя математические методы и вычислительную технику, ученые строят генные сети, моделируют биохимические и иные клеточные процессы. Через 10-15 лет геномика и протеомика достигнут такого уровня, что станет возможным изучать метаболом - комплексную схему взаимодействий всех белков в живой клетке. Эксперименты на клетках и организме будут заменены на опыты с компьютерными моделями. Появится возможность создания и применения индивидуальных лекарственных средств, разработки индивидуальных профилактических мероприятий. Особенно сильное влияние новые знания окажут на биологию развития. Станет возможным получать целостное и вместе с тем достаточно детализированное представление об индивидуальных клетках, начиная от яйцеклетки и сперматозоида и вплоть до дифференцированных клеток. Это позволит впервые на количественной основе следить за взаимодействием индивидуальных клеток на разных стадиях эмбриогенеза, что всегда было заветной мечтой ученых, изучающих биологию развития. Открываются новые горизонты в решении таких проблем как канцерогенез и старение. Достижения геномики, протеомики и биоинформатики окажут решающее влияние на теорию эволюции и систематику организмов.
3 . Белковая инженерия
синтез белок ген пространственный
Физические и химические свойства природных белков часто не удовлетворяют условиям, в которых эти белки будут использоваться человеком. Требуется изменение его первичной структуры, которое обеспечит формирование белка с иной, чем прежде, пространственной структурой и новыми физико-химическими свойствами, позволяющими и в иных условиях выполнять присущие природному белку функции. Конструированием белков занимается белковая инженерия. Для получения измененного белка используют методы комбинаторной химии и осуществляют направленный мутагенез - внесение специфических изменений в кодирующие последовательности ДНК, приводящие к определенным изменениям в аминокислотных последовательностях. Для эффективного конструирования белка с заданными свойствами необходимо знать закономерности формирования пространственной структуры белка, от которой зависят его физико-химические свойства и функции, то есть необходимо знать как первичная структура белка, каждый его аминокислотный остаток влияет на свойства и функции белка. К сожалению, для большинства белков неизвестна третичная структура, не всегда бывает известно, какую именно аминокислоту или последовательность аминокислот нужно изменить, чтобы получить белок с нужными свойствами. Уже сейчас ученые с помощью компьютерного анализа могут предсказывать свойства многих белков, исходя из последовательности их аминокислотных остатков. Подобный анализ значительно упростит процедуру создания нужных белков. Пока же для того, чтобы получить измененный белок с нужными свойствами, идут в основном иным путем: получают несколько мутантных генов и находят тот белковый продукт одного из них, который обладает нужными свойствами.
Для направленного мутагенеза используют разные экспериментальные подходы. Получив измененный ген, его встраивают в генетическую конструкцию и вводят ее в прокариотические или эукариотические клетки, осуществляющие синтез белка, кодируемого этой генетической конструкцией.
Потенциальные возможности белковой инженериизаключаются в следующем.
Изменив прочность связывания преобразуемого вещества - субстрата - с ферментом, можно повысить общую каталитическую эффективность ферментативной реакции.
Повысив стабильность белка в широком диапазоне температур и кислотности среды, можно использовать его в условиях, при которых исходный белок денатурирует и теряет свою активность.
Создав белки, способные функционировать в безводных растворителях, можно осуществлять каталитические реакции в нефизиологических условиях.
4.Изменив каталитический центр фермента, можно повысить его специфичность и уменьшить число нежелательных побочных реакций
5.Повысив устойчивость белка к расщепляющим его ферментам, можно упростить процедуру его очистки.
б.Изменив белок таким образом, чтобы он мог функционировать без обычного для него не аминокислотного компонента (витамина, атома металла и т.п.), можно использовать его в некоторых непрерывных технологических процессах.
7.Изменив структуру регуляторных участков фермента, можно уменьшить степень его торможения продуктом ферментативной реакции по типу отрицательной обратной связи и тем самым увеличить выход продукта.
8.Можно создать гибридный белок, обладающий функциями двух и более белков. 9.Можно создать гибридный белок, один из участков которого облегчает выход гибридного белка из культивируемой клетки или извлечение его из смеси.
Познакомимся с некоторыми достижениями генной инженерии белков.
1.Заменив несколько аминокислотных остатков лизоцима бактериофага Т4 на цистеин получен фермент с большим числом дисульфидных связей, благодаря чему этот фермент сохранил свою активность при более высокой температуре.
2.Замена остатка цистеина на остаток серина в молекуле р-интерферона человека, синтезируемого кишечной палочкой, предотвращала образование межмолекулярных комплексов, при котором примерно в 10 раз уменьшалась противовирусная активность этого лекарственного средства.
3.Замена остатка треонина на остаток пролина в молекуле фермента тирозил-тРНК-синтетазы повысило каталитическую активность этого фермента в десятки раз: он стал быстрее присоединять тирозин к тРНК, переносящей эту аминокислоту в рибосому в ходе трансляции.
4.Субтилизины - богатые серином ферменты, расщепляющие белки. Они секретируются многими бактериями и широко используются человеком для биодеградации. Они прочно связывают атомы кальция, повышающие их стабильность. Однако в промышленных процессах присутствуют химические соединения, которые связывают кальций, после чего субтилизины теряют свою активность. Изменив ген, ученые удалили из фермента аминокислоты, участвующие в связывании кальция, и заменили одну аминокислоту на другую с целью повышения стабильности субтилизина. Измененный фермент оказался стабильным и функционально активным в условиях, близких к промышленным.
5.Была показана возможность создания фермента, функционирующего по типу рестриктаз, расщепляющих ДНК в строго определенных местах. Ученые создали гибридный белок, один фрагмент которого узнавал определенную последовательность нуклеотидных остатков в молекуле ДНК, а другой расщеплял ДНК в этом участке.
6.Активатор тканевого плазминогена - фермент, который используют в клинике для растворения сгустков крови. К сожалению, он быстро выводится из системы кровообращения и его приходится вводить повторно или в больших дозах, что приводит к побочным эффектам. Внеся три направленные мутации в ген этого фермента, получили долгоживущий фермент, обладающий повышенным сродством к разрушаемому фибрину и с такой же фибринолитической активностью, как у исходного фермента.
7.Произведя замену одной аминокислоты в молекуле инсулина, ученые добились того, что при подкожном введении этого гормона больным, страдающим диабетом, изменение концентрации этого гормона в крови было близко к физиологическому, возникающему после приема пищи.
8.Существует три класса интерферонов, обладающих противовирусной и противораковой активностью, но проявляющих разную специфичность. Заманчиво было создать гибридный интерферон, обладающий свойствами интерферонов трех типов. Были созданы гибридные гены, включающие в себя фрагменты природных генов интерферонов нескольких типов. Часть этих генов, будучи встроенными в бактериальные клетки, обеспечивали синтез гибридных интерферонов с большей, чем у родительских молекул, противораковой активностью.
9.Природный гормон роста человека связывается не только с рецептором этого гормона, но и с рецептором другого гормона - пролактина. Для того, чтобы избежать нежелательных побочных эффектов в процессе лечения, ученые решили устранить возможность присоединения гормона роста к пролактиновому рецептору. Они добились этого, заменив некоторые аминокислоты в первичной структуре гормона роста с помощью генетической инженерии.
10. Разрабатывая средства против ВИЧ-инфекции, ученые получили гибридный белок, один фрагмент которого обеспечивал специфическое связывание этого белка только с пораженными вирусом лимфоцитами, другой фрагмент осуществлял проникновение гибридного белка внутрь пораженной клетки, а еще один фрагмент нарушал синтез белка в пораженной клетке, что приводило к ее гибели.
Таким образом, мы убедились в том, что, изменяя специфические участки белковой молекулы, можно придавать новые свойства уже существующим белкам и создавать уникальные ферменты.
Белки являются основной мишенью для лекарственных средств. Сейчас известно около 500 мишеней для действия лекарств. В ближайшие годы их число возрастет до 10 000, что позволит создать новые, более эффективные и безопасные лекарства. В последнее время разрабатываются принципиально новые подходы поиска лекарственных средств: в качестве мишеней рассматриваются не одиночные белки, а их комплексы, белок -белковые взаимодействия и фолдинг белков.
Размещено на сайт
Подобные документы
Типы взаимодействия неаллельных генов. Теория Ф. Жакоба и Ж. Моно о регуляции синтеза и-РНК и белков. Дигибридное скрещивание при неполном доминировании. Неаллельные взаимодействия генов. Механизм регуляции генетического кода, механизм индукции-репрессии.
реферат , добавлен 29.01.2011
Дифференциальная экспрессия генов и ее значение в жизнедеятельности организмов. Особенности регуляции активности генов у эукариот и их характеристики. Индуцибельные и репрессибельные опероны. Уровни и механизмы регуляции экспрессии генов у прокариот.
лекция , добавлен 31.10.2016
Механизмы функционирования живых систем. Разработка новых биотехнологических ферментов. Решение парадокса Левинталя. Сложности моделирования белков. Методы моделирования пространственной структуры белка. Ограничения сопоставительного моделирования.
реферат , добавлен 28.03.2012
Положения биологической гипотезы Жакоба-Мано. Роль генов-регуляторов в синтезе белков. Особенности протекания первого этапа этого процесса – транскрипции. Трансляция как следующая ступень их биосинтеза. Основы ферментативной регуляции этих процессов.
презентация , добавлен 01.11.2015
Физические, биологические и химические свойства белков. Синтез и анализ белков. Определение первичной, вторичной, третичной и четвертичной структуры белков. Денатурация, выделение и очистка белков. Использование белков в промышленности и медицине.
реферат , добавлен 10.06.2015
Понятие, стратегия, история развития и достижения белковой инженерии. Потенциальные возможности её использования. Механизм осуществления сайт-специфического мутагенеза. Получение модифицированных вариантов природных белков. Библиотеки пептидов и эпитопов.
курсовая работа , добавлен 19.12.2015
Физические методы исследования строения белков. Зависимость биологической активности белков от их первичной структуры. Уравнение реакции переаминирования гистидина и глиоксиловой кислоты. Биологически активные производные гормона адреналина, их биосинтез.
контрольная работа , добавлен 10.07.2011
Изучение кодирования аминокислотной последовательности белков и описание процесса синтеза белка в рибосомах. Генетический код и синтез рибонуклеиновой кислоты. Построение цепи матричной РНК и синтез протеина. Трансляция, сворачивание и транспорт белков.
реферат , добавлен 11.07.2015
Роль белков в сигнальных системах клеток, при иммунном ответе и в клеточном цикле. Виды белков в живых клетках: ферменты, транспортные, пищевые, запасные, сократительные, двигательные, структурные, защитные и регуляторные. Доменная структура белков.
презентация , добавлен 18.10.2014
Понятие белков как высокомолекулярных природных соединений (биополимеров), состоящих из остатков аминокислот, которые соединены пептидной связью. Функции и значение белков в организме человека, их превращение и структура: первичная, вторичная, третичная.
СТАТИЧЕСКАЯ БИОХИМИЯ
Глава IV .2.
Белки
Белки – неразветвляющиеся полимеры, минимальная структурная единица которых – аминокислота (АК). Аминокислоты соединены между собой пептидной связью. В природе встречается гораздо больше АК, чем входит в состав животных и растительный белков. Так, множество «небелковых» АК содержится в пептидных антибиотиках или являются промежуточными продуктами обмена белков. В состав белков входит 20 АК в альфа-форме, расположенных в различной, но строго определенной для каждого белка последовательности.
Классификация АК
По химическому строению
1) Алифатические – глицин (Гли), аланин (Ала), валин (Вал), лейцин (Лей), изолейцин (Илей);
2) Оксикислоты – серин (Сер), треанин (Тре);
3) Дикарбоновые – аспарагин (Асп), глутамин (Глу), аспарагиновая кислота (Аск), глутаминовая кислота (Глк);
4) Двуосновные – лизин (Лиз), гистидин (Гис), аргинин (Арг);
5) Ароматические – фениналанин (Фен), тирозин (Тир), триптофан (Три);
6) Серосодержащие – цистеин (Цис), метионин (Мет).
По биохимической роли:
1) глюкогенные – через ряд химических превращений поступают на путь гликолиза (окисления глюкозы) – Гли, Ала, Тре, Вал, Аск, Глк, Арг, Гис, Мет.
2) кетогенные – участвуют в образовании кетоновых тел - Лей, Илей, Тир, Фен.
По заменимости:
1) Незаменимые – не синтезируются в организме – Гис, Иле, Лей, Лиз, Мет, Фен, Тре, Три, Вал, а у молодняка Арг, Гис.
2) Заменимые – остальные.
За счет наличияв молекуле АК одновременно аминной и карбоксильной групп этим соединениям присущи кислотно-основные свойства. В нейтральной среде АК существуют в виде биполярных ионов- цвиттер-ионов т.е.
не NH 2 – R – COOH , аNH 3 + – R - COO –
Образование пептидной связи . Если карбоксильная группа одной АК ацилирует аминогруппу другой АК, от образуется амидная связь, которую называют пептидной. Т. о. пептиды – это соединения, образованные из остатков альфа-АК, соединенных между собой пептидной связью .
Данная связь достаточно стабильна и разрыв ее происходит лишь при участии катализаторов – специфических ферментов. Посредством такой связи АК объединяются в достаточно длинные цепочки, которые носят название полипептидных. Каждая такая цепь содержит на одном конце АК со свободной аминогруппой – это N -концевой остаток, и на другом с карбоксильной группой – С-концевой остаток.
Полипептиды, способные самопроизвольно формировать и удерживать определенную пространственную структуру, которая называется конформацией, относят к белкам. Стабилизация такой структуры возможна лишь при достижении полипептидами определенной длины, поэтому белками обычно считают полипептиды молекулярной массой более 5 000 Да. (1Да равен 1/12 изотопа углерода). Только имея определенное пространственное строение, белок может функционировать.
Функции белков
1) Структурная (пластическая) – белками образованы многие клеточные компоненты, а в комплексе с липидами они входят в состав клеточных мембран.
2) Каталитическая – все биологические катализаторы – ферменты по своей химической природе являются белками.
3) Транспортная – белок гемоглобин транспортирует кислород, ряд других белков образуя комплекс с липидами транспортируют их по крови и лимфе (пример: миоглобин, сывороточный альбумин).
4) Механохимическая – мышечная работа и иные формы движения в организме осуществляются при непосредственном участии сократительных белков с использованием энергии макроэргических связей (пример: актин, миозин).
5) Регуляторная – ряд гормонов и других биологически активных веществ имеют белковую природу (пр.: инсулин, АКТГ).
6) Защитная – антитела (иммуноглобулины) являются белками, кроме тогооснову кожи составляет белок коллаген, а волос – креатин. Кожа и волосы защищают внутреннюю среду организма от внешних воздействий. В состав слизи и синовиальной жидкости входят мукопротеиды.
7) Опорная – сухожилия, поверхности суставов соединения костей образованы в значительной степени белковыми веществами (пр.: коллаген, эластин).
8) Энергетическая – аминокислоты белков могут поступать на путь гликолиза, который обеспечивает клетку энергией.
9) Рецепторная – многие белки участвуют в процессах избирательного узнавания (рецепторы).
Уровни организации белковой молекулы.
В современной литературе принято рассматривать4 уровня организации структуры молекулы белка.
Последовательность аминокислотных остатков, соединенных между собой пептидной связью называют первичным уровнем организации белковой молекулы. Она кодируется структурным геном каждого белка. Связи: пептидная и дисульфидные мостики между относительно близко расположенными остатками цистеинов. Это ковалентные взаимодействия, которые разрушаются только под действием протеолитических ферментов (пепсин, трипсин и т.д.).
Вторичной структурой называют пространственное расположение атомов главной цепи молекулы белка . Существует три типа вторичной структуры: альфа-спираль, бета-складчатость и бета-изгиб. Образуется и удерживается в пространстве за счет образования водородных связей между боковыми группировками АК основной цепи. Водородные связи образуются между электроотрицательными атомами кислорода карбонильных групп и атомами водорода двух аминокислот.
Альфа-спираль – это пептидная цепь штопорообразно закрученная вокруг воображаемого цилиндра. Диаметр такой спирали 0,5 А. В природных белках обнаружена только правая спираль. Некоторые белки (инсулин) имеют две параллельные спирали. Бета-складчатость – полипептидная цепь собрана в равнозначные складки. Бета-изгиб – образуется между тремя аминокислотами за счет водородной связи. Он необходим для изменения пространственного расположения полипептидной цепи при образовании третичной структуры белка.
Третичная структура – это свойственный данному белку способ укладки полипептидой цепи в пространстве . Это основа функциональности белка. Она обеспечивает стабильность обширных участков белка, состоящих из множества аминокислотных остатков и боковых групп. Такие упорядоченные в пространстве участки белка формируют активные центры ферментов или зоны связывания и повреждение третичной структуры приводит к утрате функциональной активности белка.
Стабильность третичной структуры зависит в основном от нековалентных взаимодействий внутри белковой глобулы – преимущественно водородных связей и ван-дер-ваальсовых сил. Но некоторые белки дополнительно стабилизируются за счет таких ковалентных взаимодействий как дисульфидные мостики межу остатками цистеина.
Большинство белковых молекул имеют участки как альфа-спирали так и бета-складчатости. Но чаще по форме третичной структуры разделяют глобулярные белки – построенные преимуществено из альфа-спиралей и имеющеие форму шара или элипса (большинство ферментов). И фибрилярные – состоящие пеимущественно из бета-складчатости и имеющие сплющенную или нитевидную формы (пепсин, белки соединительной такни и хряща).
Размещение в пространстве взаимодействующих между собой субъединиц, образованных отдельными полипептидными цепями, называется четвертичной структурой . Т.е. в формировании четвертичной структуры участвуют не пептидные цепи сами по себе, а глобулы, образованные каждой из этих цепей в отдельности. Четвертичная структура – это высший уровень организации белковой молекулы и он присущ далеко не всем белкам. Связи, формирующие эту структуру нековалентные: водородные, электростатического взаимодействия.
Фундаментальный принцип молекулярной биологии: последовательность аминокислотных остатков полипептидной цепи белка несет в себе всю информацию, которая необходима для формирования определенной пространственной структуры. Т.е. имеющаяся в данном белке аминокислотная последовательность предопределяет образование альфа- или бета-конформации вторичной структуры за счет образования между этими АК водородных или дисульфидных связей и в дальнейшем формирование глобулярной или фибрилярной структуры также за счет нековалентных взаиомдействий между боковыми учатками определенных аминокислот.
Физико-химические свойства
Растворы белка относятся к растворам ВМС и обладают рядом свойств гидрофильных коллоидов: медленной диффузией, высокой вязкостью, опаслеценцией, дают конус Тиндаля.
1) Амфотерность связана с наличием в молекуле белка катионообразующих групп – аминогрупп и анионообразующих – карбоксильных группу. Знак заряда молекулы зависит от количества свободных групп. Если преоблазают карбоксильные группы то заряд молекулы отрицательный (проявляются свойства слабой кислоты), если аминогруппы – то положительный (основные свойства).
Заряд белка также зависит от рН среды. В кислой среде молекула приобретаетположительный заряд, в щелочной – отрицательный.
[ NH 3 + - R – COO - ] 0
pH > 7 [ OH - ]7 >pH [ H + ]
[ NH 2 - R – COO - ] - [ NH 3 + - R – COOH] +
Значение рН при котором число разноименных зарядов в белковой молекуле одинаково, т. е. суммарный заряд равен нулю называется изоэлектрической точкой данного белка. Устойчивость белковой молекулы к воздействию физических и химических факторов в изоэлектрической точке наименьшая.
Большинство природных белков содержат значительное количество дикарбоновых аминокислот и поэтому относятся к кислым белкам. Их изоэлектрическая точка лежит в слабокислой среде.
2) Растворы белков обладают буферными свойствами за счет их амфотерности.
3) Растворимость . Поскольку молекула белка содержит полярные амино – и карбоксильные группы, то в растворе поверхностные остатки АК гидратируются – происходит образование коацервата .
4) Коацервация - слияние водных оболочек нескольких частиц, без объединения самих частиц.
5) Коагуляция – склеивание белковых частиц и выпадение их в осадок. Это происходит при удаленииих гидратной оболочки. Для этого достаточно изменить структуручастицы белка, так, чтобы ее гидрофильные группы, которые связывают воду растворителя, оказались внутри частицы. Реакции осаждения балка в растворе делятся на две группы: обратимые (высаливание) и необратимые (денатурация).
6) Денатурацией называется существенное изменение вторичной и третичной структуры белка, т. е. Нарушение системы нековалентных взаимодействий, не затрагивающее его ковалентной (первичной) структуры. Денатурированный белок лишен всякой биологической активности в клетке и в основном используется как источник аминокислот. Денатурирующими агентами могут быть химические факторы: кислоты, щелочи, легко гидратирующие соли, органические растворители, различные окислители. К физическим факторам могут быть отнесены: действие высокого давления, многократное замораживание и оттаивание, ультразвуковые волны, УФ-лучи, ионизирующая радиация. Но наиболее распространенным физическим фактором денатурации белка является повышение температуры.
В ряде случаев денатурированный белок в клетке может быть подвергнут ренатурации, т. е. свернут обратно в первоначальную пространственную структуру. Этот процесс происходит при участии специфических белков, так называемых белков теплового шока (heat shock proteins или hsp ) молекулярной массой 70 кДа. Данные белки синтезируются в клетках в большом количествепри воздействии на нее (или весь организм) неблагоприятных факторов, в частности повышенной температуры. Присоединяясь к развернутой полипептидной цепи hsp 70 быстро сворачивают ее в правильную первоначальную структуру.
Классификация белков
По растворимости: водорастворимые, солерстворимые, спирторастворимые, нерастворимые и пр.
По конформационной структуре : фибриллярные, глобулярные.
По химическому строению: протеины – состоят только из аминокислот, протеиды – помимо АК имеют в составе небелковую часть (углеводы, липиды, металлы, нуклеиновые кислоты)
Протеины :
1) Альбумины – растворимы в воде, не растворимы в конц. растворах солей. р I = 4.6-4.7. Существуют альбумины молока, яиц, сыворотки крови.
2) Глобулины – не растворимы в воде, растворимы в солевых растворах. Имунноглобулины .
3) Гистоны – растворимы в воде, в слабоконцентрированных кислотах. Обладают выраженными основными свойствами. Это ядерные белки, они связаны с ДНК и РНК.
4) Склеропротеины – белки опорных тканей (хрящей, костей), шерсти, волос. Не растворимы в воде, слабых кислотах и щелочах.
а) коллагены – фибрилярные белки соединительной ткани. При длительном кипячении они растворяются в воде и при застудневании образуется желатин.
б) эластины– белки связок и сухожилий. По свойствам похожи на коллагены, но подвергаются гидролизу под действием ферментов пищеварительного сока;
в) кератин – входит в состав волос, перьев, копыт;
г) фиброин – белок шелка, в совем составе содержит много серина;
д) проламины и глютенины – белки растительного происхождения.
Протеиды
Помимо АК содержат простетическую группу и в зависимости от ее химической природы они классифицируются на:
1) Нуклеопротеиды – простетическая група – нуклеиновые кислоты. Среди многочисленных классов нуклеопротеидов наиболее изученными являются рибосомы, состоящие из нескольких молекул РНК и рибосомных белков, и хроматин – основной нуклеопротеид эукариотических клеток, состоящий из ДНК и структурообразующих белков – гистонов (содержатся в клеточном ядре и митохондриях) (подробнее см. главы "Нуклеиновые кислоты" и "Матричный биосинтез").
2) Гемопротеиды - небелковый компонент этих протеидов – гем, построен из четырех пиррольных колец, с ними связан ион двухвалентного железа (через атомы азота). К таким белка относятся: гемоглобин, миоглобин, цитохромы. Этот класс белков еще называют хромопротеиды, поскольку гем является окрашенным соединением. Гемоглобин – транспорт кислорода. Миоглобин – запасание кислорода в мышцах. Цитохромы (ферменты) – катализ окислительно-восстановаительных реакций и электронный транспорт в дыхательной цепи.
(Подробнее см. приложение 1).
3) Металлопротеиды – в состав простетической группы входят металлы. Хлорофилл – содержит гем, но вместо железа – магний. Цитохром а – содержит медь, сукцинатдегидрогеназа и др. ферменты содержат негеминовое железо (ферродоксин ).
4) Липопротеиды – содержат липиды, входят в состав клеточных мембран
5) Фосфопротеиды – содержат остаток фосфорной кислоты
6) Глюкопротеиды – содержат сахара
ЛИТЕРАТУРА К ГЛАВЕ IV .2.
1. Балезин С. А. Практикум по физической и коллоидной химии // М:. Просвещение, 1972, 278 с.;
2. Бышевский А. Ш., Терсенов О. А. Биохимия для врача // Екатеринбург: Уральский рабочий, 1994, 384 с.;
3. Кнорре Д. Г., Мызина С. Д. Биологическая химия. – М.: Высш. шк. 1998, 479 с.;
4. Молекулярная биология. Структура и функции белков /Под ред. А. С. Спирина // М.: Высш. шк., 1996, 335 с.;
6. Равич – Щербо М. И., Новиков В. В. Физическая и коллоидная химия // М:. Высш. шк., 1975,255 с.;
7. Филиппович Ю. Б., Егорова Т. А., Севастьянова Г. А. Практикум по общей биохимии // М.: Просвящение, 1982, 311с.;
Тема: Белки - природные биополимеры
“Меняя каждый миг свой образ прихотливый,
капризна, как дитя, и призрачна, как дым,
кипит повсюду жизнь в тревоге суетливой,
великое смешав с ничтожным и смешным…”
С.Я. Надсон
| Методическая информация |
||||||||||||||||||||||||||||||
| Тип занятия | Интегрированный (биология + химия) проблемно-исследовательский мультимедиа урок |
|||||||||||||||||||||||||||||
| Формировать у обучающихся представление о свойствах и функциях белков в клетке и организме |
||||||||||||||||||||||||||||||
| Обучающие: дать понятие о белках - природных биополимерах, их многообразных функциях, химических свойствах белков; формировать знания об уникальных особенностях строения белков; углубить знания о взаимосвязи строения и функции веществ на примере белков; учить обучающихся, использованию знаний смежных предметов для получения более полной картины мира. Развивающие: развитие познавательного интереса, установление межпредметных связей; совершенствовать умения анализировать, сравнивать, устанавливать взаимосвязь между строением и свойствами. Воспитательные: показать материальное единство органического мира; формирование научного мировоззрения; |
||||||||||||||||||||||||||||||
| Метод проблемного изложения, частично-поисковый, эвристический, исследовательский |
||||||||||||||||||||||||||||||
| Функция преподавателя: | Управляющий поисковой работой обучающихся, консультант |
|||||||||||||||||||||||||||||
| Знания, умения, навыки и компетенции, которые обучающиеся актуализируют, приобретут, закрепят в ходе занятия: | Формируются такие мыслительные операции, как: сравнение свойств белка, классификация структур белковой молекулы, сравнительный анализ функций белка. Основные понятия: Аминокислоты, пептидная связь, полипептид, структура белка, функции белка, свойства белка, денатурация. Основные навыки: Работа с химическим оборудованием, работа по выявлению активности каталазы |
|||||||||||||||||||||||||||||
| Необходимое оборудование и материалы: | Компьютер, презентация по теме урока. Эксперимент: пробирки, штативы, спиртовка, держатель. Реактивы и материалы: р-р Белка куриного яйца, азотная кислота, р-р сульфата меди(II), щелочь, раствор 3% перекиси водорода, сырой и вареный картофель или мясо. |
|||||||||||||||||||||||||||||
| Ведущий тип деятельности: | Продуктивный, творческий, проблемный |
|||||||||||||||||||||||||||||
| Технологическая карта занятия |
||||||||||||||||||||||||||||||
| Мотивация: | Как изучение этой темы может вам помочь в вашей будущей профессии? |
|||||||||||||||||||||||||||||
| Ход занятия: |
||||||||||||||||||||||||||||||
| Организационный момент | “Белки, жиры и углеводы, |
|||||||||||||||||||||||||||||
| Актуализация знаний | А знаете ли Вы: 8. Как появилась жизнь на Земле? Что лежит в основе жизни? Вот сегодня мы об этом и будем вести речь. План занятия: Определение. Функции белков. Состав и строение белков. Структура белков. Химические свойства белков. 6. Превращение белков в организме. |
|||||||||||||||||||||||||||||
| Проблемный вопрос? Как строение белка может быть связано с его свойствами и функциями? Гипотеза: Примеры белков История открытия: Состав белков Определение | Понять, каким образом белки осуществляют перечисленные выше многообразные функции, непросто. Единственный способ приблизиться к решению этой задачи - узнать, из чего построен белок, как расположены структурные элементы, составляющие его молекулу, по отношению друг к другу и в пространстве, как они взаимодействуют друг с другом и веществами внешней среды, т.е. изучить строение и свойства белков. |
|||||||||||||||||||||||||||||
| Раскрыть причинно- следственную зависимость: функции - строение. белки - полимеры, мономеры - аминокислоты |
||||||||||||||||||||||||||||||
| Назовите известные вам белки, укажите их местонахождение? глобулин - вакцина, родопсин - зрительный пурпур, В середине 19 века положено начало изучения белков, но только через 100 лет учёные систематизировали белки, определи их состав, а также сделали вывод, что белки - это главный компонент живых организмов. А.Я. Данилевский - наличие в белке пептидной связи Э.Фишер - синтезировал соединения белка Химический состав белка может быть представлен следующими данными: С -55%, О - 24%, Н - 7,3%, N - 19%, S -2,4%. На долю белков приходится более 50% общей массы органических соединений животной клетки: в мышцах - 80%, в коже - 63%, в печени - 57%, в мозге - 45%, в костях -28% Химические формулы некоторых белков : Пенициллин С16Н18О4N2 Казеин С1864Н3021О576N468 S2 Гемоглобин С3032Н4816 О872N780S8Fе4 - Давайте дадим определение термину БЕЛОК БЕЛКИ - биополимеры нерегулярного строения, мономерами которого являются 20 аминокислот разных типов. В химический состав аминокислот входят: С, О, Н, N, S. Белковые молекулы могут образовывать четыре простраственные структуры и выполняют в клетке и организме целый ряд функций: строительную, каталитическую, регуляторную, двигательную, транспортную |
||||||||||||||||||||||||||||||
| Функции белков | - Белки - основа живого на Земле, входят в состав кожи, мышечной и нервной ткани, волос, сухожилий, стенок сосудов животных и человека; это строительный материал клетки. Роль белков трудно переоценить, т.о. жизнь на нашей планете действительно можно рассматривать как способ существования белковых тел, осуществляющих обменом веществ и энергией с внешней средой. Поскольку белок содержит разнообразные функциональные группы, он не может быть отнесен к какому-нибудь из ранее изученных классов соединений. В нем как в фокусе сочетаются признаки соединений, относящихся к различным классам. Отсюда его многообразие. Это в сочетании с особенностями его структуры и характеризует белок как высшую форму развития вещества. |
|||||||||||||||||||||||||||||
| Структура белка | Составить конспект и ответить в процессе беседы на вопросы: Остатки каких аминокислот входят в состав молекул белка? (см.прил.) За счёт каких функциональных групп аминокислот происходит соединение их друг с другом? Что понимают под «первичной» структурой белка? Что представляет собой «вторичная» структура белка? Какие связи её удерживают? Что такое «третичная» структура? За счет, каких связей она образуется? В чем особенность четвертичной структуры? (В виде линейной последовательности аминокислот)
-Что собой представляет первичная структура белка? Какие связи стабилизируют вторичную структуру? (Пространственная конфигурация белковой молекулы свернутые в виде спирали. В формировании спиральной конфигурации полипептидной цепи играют роль водородные связи между -С=О и -N-H группами.. )
- Что собой представляет третичная структура белка ? (Э то конфигурация в виде закрученной вспираль полипептидной цепи. Она поддерживается взаимодействием разных функциональных групп полипептидной цепи. Так, между атомами серы образуется дисульфидный мостик, между карбоксильной и гидроксильной группами имеется сложноэфирный мостик, а между карбоксильной и аминогруппами может возникнуть солевой мостик. Для этой структуры характерны и водородные связи).
- Что собой представляет четвертичная структура белка? (Некоторые белковые макромолекулы могут соединяться друг с другом и образовывать относительно крупные агрегаты- макромолекулы белка).
Какие химические свойства будут характерны для белков? (Амфотерность связана с наличием в молекуле белка катионообразующих групп - аминогрупп и анионообразующих - карбоксильных группу. Знак заряда молекулы зависит от количества свободных групп. Если преобладают карбоксильные группы, то заряд молекулы - отрицательный (проявляются свойства слабой кислоты), еслиаминогруппы - то положительный (основные свойства)).
|
|||||||||||||||||||||||||||||
| Химические свойства белков | Для белков характерны реакции, в результате которых выпадает осадок. Но в одних случаях полученный осадок при избытке воды растворяется, а в других - происходит необратимое свертывание белков, т.е. денатурация. Происходит изменение вторичной, третичной и четвертичной структур белковой макромолекулы под влиянием внешних факторов: температура, действия химических реагентов, механического воздействия. При денатурации изменяются физические свойства белка, снижается растворимость, теряется биологическая активность К чему может привести денатурация? Нарушение антигенной чувствительности белка; Блокирование ряда иммунологических реакций; Нарушение обмена веществ; Воспаление слизистой оболочки ряда органов пищеварения (гастриты, колит); Камнеобразование (камни имеют белковую основу). Также для белков характерны: Свертывание белков при нагревании Осаждение белков солями тяжелых металлов и спиртом Белки горят с образованием азота, углекислого газа и воды, а также некоторых других веществ. Горение сопровождается характерным запахом жженых перьев. Белки подвергаются гниению (под действием гнилостных бактерий), при этом образуются метан (CH4), сероводород (H2S), аммиак (NH3), вода и другие низкомолекулярные продукты. Амфотерность Строение АК в общем виде: NH2-CH- COOH, где R - углеводородный радикал. СООН - карбоксильная группа / кислотные свойства/. NН2 - аминогруппа / основные свойства/. Процесс восстановления структуры белка называется ренатурацией Превращения белков в организме. Белки пищи → полипептиды → α-аминокислоты → белки организма |
|||||||||||||||||||||||||||||
| Как ведет себя белок по отношению к воде? |
|
|||||||||||||||||||||||||||||
| Гидролиз | Гидролиз белка - разрушение первичной структуры белка под действием кислот, щелочей или ферментов, приводящее к образованию α- аминокислот, из которых он был составлен.
Белки - Альбумозы - Дипептиды - Аминокислоты |
|||||||||||||||||||||||||||||
| Качественные, цветные реакции на белок | Ксантопротеиновая реакция - реакция на ароматические циклы. Белок + HNO3(к) → белый осадок → желтая окраска → оранжевая окраска + NH3 Как с помощью ксантопротеиновой реакции можно отличить натуральные шерстяные нитки от искусственных? |
|||||||||||||||||||||||||||||
| Биуретовая реакция - реакция на пептидные связи. Белок + Cu(OH)2 → фиолетовая окраска раствора Можно ли с помощью химии решить проблему дефицита белковой пищи? Должна медленно появиться розово-фиолетовая или пурпурная окраска. Это реакция на пептидные связи в соединениях. В присутствии разбавленного раствора Си в щелочной среде атомы азота пептидной цепи образуют окрашенный в пурпурный цвет комплекс с ионами меди (II). Биурет (производное мочевины) тоже содержит группу CONH - и поэтому дает эту реакцию. |
||||||||||||||||||||||||||||||
| Функции белка |
|
|||||||||||||||||||||||||||||
| Домашняя работа | Один стакан цельного молока содержит 288 мг кальция. Сколько нужно выпивать в день молока для снабжения вашего организма достаточным количеством этого элемента? Суточная потребность 800 мг Са. (Ответ. Для удовлетворения суточной потребности в кальции взрослый мужчина должен выпивать в день 2,7 стакана молока: 800 мг Са*(1 стакан молока/ 288 Са) = 2,7 стакана молока). В куске белого пшеничного хлеба 0,8 мг железа. Сколько кусков нужно съедать в день для удовлетворения суточной потребности в этом элементе. (Суточная потребность в железе 18 мг). (Ответ. 22,5 кусочка) 18 мг.: 0,8= 22,5 |
|||||||||||||||||||||||||||||
| Закрепление изученного материала Игра «Подними руку, если согласен» | Сейчас вы будете выполнять задание по изученной теме в виде теста. (Во время проверки обучающиеся меняются своими работами и оценивают работу соседа. Варианты правильных ответов на доске. По окончании проверки каждый выставляет оценку соседу) - Какая структура является самой прочной? Почему?
-Как можно с помощью проволоки, бус показать образование вторичной, третичной, четвертичной структур белка . За счет каких связей, взаимодействий это происходит? А теперь с помощью теста проверим, как вы усвоили материал. На ответ «Да» поднимаете руку. 1. В состав белков входят аминокислоты, прочно связанные между собой водородными связями (Нет) 2. Пептидной называют связь между углеродом карбоксильной группы одной аминокислоты и азотом аминогруппы другой аминокислоты. (Да) 3. Белки составляют основную часть органических веществ клетки. (Да) 4.Белок - мономер. (Нет) 5. Продукт гидролиза пептидных связей - вода. (Нет) 6. Продукты гидролиза пептидных связей - аминокислоты. (Да) 7. Белок - макромолекула. (Да) 8. Катализаторы клетки - это белки. (Да) 9. Существуют белки, переносящие кислород и углекислый газ. (Да) 10. Иммунитет не связан с белками. (Нет) |
|||||||||||||||||||||||||||||
| Высказывания о жизни и белках знаменитых людей | «Повсюду, где мы встречаем жизнь, мы находим, что она связана с каким-либо белковым телом». Ф.Энгельс «Анти-Дюринг» Знаменитый путешественник и естествоиспытатель Александр Гумбольдт еще на пороге 19 века давал такое определение жизни: «Жизнь есть способ существования белковых тел, существенным моментом которого является постепенный обмен веществ с окружающей их внешней природой; причем с прекращением этого обмена веществ прекращается и сама жизнь, что приводит к разложению белка». Определение, данное Ф.Энгельсом в работе«Анти-Дюринг», позволяет задуматься над тем, как современная наука представляет процесс жизни. «Жизнь - это переплетение сложнейших химических процессов взаимодействия белков между собой и другими веществами». |
|||||||||||||||||||||||||||||
Приложение № 1
Функции белков.
Каталитическая функция
Белок как фермент: Ферменты - белки, обладающие каталитической активностью, т.е. ускоряющие протекание реакций. Все ферменты катализируют только одну реакцию. Заболевания, вызываемые ферментной недостаточностью.
Пример: неперевариваемость молока (нет фермента лактазы); гиповитаминозы (витаминная недостаточность)
Определение активности ферментов в биологических жидкостях имеет большое значение для диагностики заболевания. Например, по активности ферментов в плазме крови определяют вирусный гепатит.
Ферменты используют как реактивы при диагностике некоторых заболеваний.
Ферменты используют для лечения некоторых болезней. Примеры: панкреатин, фестал, лидаза.
Ферменты используются в промышленности: при приготовлении безалкогольных напитков, сыров, консервов, колбас, копченостей.
Ферменты используются при обработке льна, конопли, для смягчения кожи в кожевенной промышленности, они входят в состав стиральных порошков.
Структурная функция
Белки являются структурным компонентом многих клеток. Например, мономеры актина итубулина — это глобулярные, растворимые белки, но после полимеризации они формируют длинные нити, из которых состоит цитоскелет, позволяющий клетке поддерживать форму.Коллаген и эластин — основные компоненты межклеточного вещества соединительной ткани (например, хряща), а из другого структурного белка кератина состоят волосы, ногти,перья птиц и некоторые раковины.
Защитная функция
Существуют несколько видов защитных функций белков:
Физическая защита. В ней принимает участие коллаген — белок, образующий основу межклеточного вещества соединительных тканей (в том числе костей, хряща, сухожилий и глубоких слоёв кожи (дермы)); кератин, составляющий основу роговых щитков, волос, перьев, рогов и др. производных эпидермиса.
Химическая защита. Связывание токсинов белковыми молекулами может обеспечивать их детоксикацию. Особенно важную роль в детоксикации у человека играютферментыпечени, расщепляющие яды или переводящие их в растворимую форму, что способствует их быстрому выведению из организма.
Иммунная защита. Белки, входящие в состав крови и других биологических жидкостей, участвуют в защитном ответе организма как на повреждение, так и на атакупатогенов
Регуляторная функция
Многие процессы внутри клеток регулируются белковыми молекулами, которые не служат ни источником энергии, ни строительным материалом для клетки. Эти белки регулируюттранскрипцию, трансляцию, а также активность других белков и др.
Регуляторную функцию белки осуществляют либо за счёт ферментативной активности), либо за счёт специфического связывания с другими молекулами, как правило, влияющего на взаимодействие с этими молекулами ферментов.
Сигнальная функция
Сигнальная функция белков — способность белков служить сигнальными веществами, передавая сигналы между клетками, тканями, о́рганами и разными организмами. Часто сигнальную функцию объединяют с регуляторной, так как многие внутриклеточные регуляторные белки тоже осуществляют передачу сигналов.
Сигнальную функцию выполняют белки-гормоны, цитокины, факторы роста и др.
Транспортная функция
Примером транспортных белков можно назвать гемоглобин, который переносит кислород из лёгких к остальным тканям и углекислый газ от тканей к лёгким, а также гомологичные ему белки, найденные во всех царствах живых организмов.
Запасная (резервная) функция белков
К таким белкам относятся так называемые резервные белки, которые запасаются в качестве источника энергии и вещества в семенах растений и яйцеклетках животных; белки третичных оболочек яйца (овальбумины) и основной белок молока (казеин) также выполняют, главным образом, питательную функцию. Ряд других белков используется в организме в качестве источника аминокислот, которые в свою очередь являются предшественниками биологически активных веществ, регулирующих процессыметаболизма.
Рецепторная функция
Белковые рецепторы могут как находиться в цитоплазме, так и встраиваться в клеточную мембрану. Одна часть молекулы рецептора воспринимает сигнал, которым чаще всего служит химическое вещество, а в некоторых случаях — свет, механическое воздействие (например, растяжение) и другие стимулы. При воздействии сигнала на определённый участок молекулы — белок-рецептор — происходят её конформационные изменения. В результате меняется конформация другой части молекулы, осуществляющей передачу сигнала на другие клеточные компоненты.
Моторная (двигательная) функция
Целый класс моторных белков обеспечивает движения организма, например, сокращение мышц, в том числе локомоцию (миозин), перемещение клеток внутри организма (например, амебоидное движение лейкоцитов), движение ресничек и жгутиков, а также активный и направленный внутриклеточный транспорт создайте презентацию
Коды пищевых добавок
| Е103, Е105, Е111, Е121, Е123,Е125,Е126, Е130, Е152. |
|
| 2. Подозрительные | Е104, ЕЕ122, Е141, Е150, Е171, Е173, Е180, Е241, Е477. |
| 3. Опасные | Е102, Е110, Е120, Е124,. Е127. |
| 4.Канцерогенные | Е131,Е210-Е217,Е240, Е330. |
| 5. Вызывающие расстройства кишечника | |
| 6. Вредные для кожи | |
| 7. Вызывающие нарушение давления | |
| 8. Провоцирующие появление сыпи | |
| 9. Повышающие уровень холестерина | |
| 10. Вызывающие расстройство желудка | Е338 Е341, Е407, Е450, Е461 - Е466 |
Практическая работа
Тема: «Химические свойства белков. Качественные (цветные) реакции на белки».
Цель : Изучить химические свойства белков. Познакомиться с качественными реакциями на белки. Активность фермента каталазы в живых и мертвых тканях..
«Денатурация белков»
Порядок выполнения.
Приготовьте раствор белка.
В пробирку налейте 4-5 мл раствора белка и нагрейте до кипения.
Отметьте изменения.
Охладите содержимое пробирки и разбавьте водой.

«Ксантопротеиновая реакция»
Порядок выполнения.
2. В пробирку прилейте 1 мл уксусной кислоты.
3. Содержимое пробирки нагрейте.
4. Охладите смесь и добавьте аммиак до щелочной среды.
5. Отметьте изменения.
« Биуретовая реакция »
Порядок выполнения.
1. В пробирку налейте 2-3 мл раствора белка.
2. Добавьте 2-3 мл раствора гидроксида натрия и 1-2 мл раствора медного купороса..
3. Отметьте изменения.
Качественные (цветные)
реакции на белки. Опыты №2 и №3
Ксантопротеиновая реакция
Белок + HNO3конц > ярко?желтое окрашивание
(обнаружение бензольных ядер)
Биуретовая реакция
Белок + NaOH+CuSO4 > красно-
фиолетовое окрашивание
(обнаружение пептидных связей)
«Доказательство наличие белка только в живых организмах»
Порядок выполнения.
1. В пробирках находятся свежевыжатый сок картофеля, кусочки сырого картофеля,
вареный картофель.
2. Добавьте в каждую пробирку 2-3 мл перекиси водорода.
3. Отметьте изменения. (каталаза - ферментный белок выделяется только в
присутствии молекулярной воды, растворенные в воде альбумины сворачиваются)
| Опыт | Что делали | Что наблюдали | Объяснение и выводы |
| 1. Качественные реакции на белки. | |||
| а) Биуретовая реакция. | К 2 мл раствора белка добавить раствор сульфата меди (II) и щелочи. | Красно-фиолетовое окрашивание. | При взаимодействии растворов образуется комплексное соединение между ионами Си2+ и полипептидами. |
| б) Ксантопротеиновая реакция. | К 2 мл раствора белка добавить по каплям концентрирующуюся азотную кислоту. | Желтое окрашивание. | Реакция доказывает, что в состав белков входят остатки ароматических аминокислот. |
| 2. Денатурация белка. | Пробирку № 3 с раствором белка нагреть. | Во всех трех случаях наблюдается необратимое свертывание белка — денатурация. | При нагревании, действии неразбавленного спирта, солей тяжелых металлов происходит разрушение вторичной и третичной структуры, с сохранением первичной. |


«Жизнь есть способ существования белковых тел…» Ф.Энгельс
Опорный конспект Приложение № 2- АМФОТЕРНОСТЬ
Кислая среда = по типу щелочи
[белок]+ + ОН- = по типу кислоты
- ГИДРОЛИЗ ……разрушение первичной структуры белка до α-аминлкислот
Качественные реакции
- БИУРЕТОВАЯ РЕАКЦИЯ (распознавание в молекуле белка пептидных связей).
Б. + CuSO4 + NaOH → фиолетовое окрашивание
………………………………
- КСАНТОПРОТЕИНОВАЯ РЕАКЦИЯ (обнаружение бензольных ядер).
Б. + HNO3 → желтое окрашивание
- ГОРЕНИЕ БЕЛКА ………………………..
N2, CO2, H2O - запах жженых перьев
- ДЕНАТУРАЦИЯ - ………………………..
высокая t разрушение
радиоактивное облучение 2-3 структуры
соли тяжелых Ме
Протеины ПротеидыБЕЛКИ - важнейшая составная часть живых организмов, входят в состав кожи, роговых покровов, мышечной и нервной ткани

 (простые) (сложные)
(простые) (сложные)



| 1 вариант | 2 вариант |
| 1. В состав аминокислот входят: а) только аминогруппы б) только карбоксильные группы в) аминогруппы и карбоксильные группы г) аминогруппы и карбонильные группы | 1. Аминокислотой является вещество, формула которого: а) СН3СН2 СОNН2 б) NН2СООН в) NН2СН2СН2СООН г) NН2СН2СОН |
| 2. Аминокислоты, которые не могут синтезироваться в организме человека, а поступают только с пищей, называются а) a -аминокислотами б) пищевыми в) -аминокислотами г) незаменимыми | 2. Аминокислоты - это а) бесцветные легкокипящие жидкости б) газы тяжелее воздуха в) кристаллические вещества розового цвета г) бесцветные кристаллические вещества |
| 3. При взаимодействии аминокислот со щелочами и кислотами образуются: б) сложные эфиры в) дипептиды г) полипептиды | 3. Образование полипептидов происходит по типу реакции: а) полимеризации б) поликонденсации в) присоединения г) замещения |
| 4. Формула 3-аминопропановой кислоты: а) NН2СН2СООН б) NН2СН2СН2СООН в) NН2СН2СН2 NН2 г) NН2СН СН2СООН | 4. Самые слабые кислотные свойства проявляет кислота: а) уксусная б) хлоруксусная в) аминоуксусная г) дихлоруксусная |
| 5. Верным является утверждение, что аминокислоты это: а) твердые вещества молекулярного строения б) кристаллические вещества ионного строения в) жидкости, хорошо растворимые в воде г) кристаллические вещества с низкими температурами плавления | 5. Аминокислоты являются амфотерными соединениями, так как они взаимодействуют: а) с кислотами б) с щелочами в) со спиртами г) с кислотами и щелочами |
Ответы 1 - В, 2 - Г, 3 - А, 4 - Б, 5 - Б Ответы 1 - В, 2 - Г, 3 -Б, 4 -В, 5 - Г
| 1 вариант | 2 вариант |
| 1. Укажите название белка, выполняющего защитную функцию: | 1. Укажите название белка, выполняющего ферментативную функцию: а) гемоглобин, б) оксидаза, в) антитела. |
| 2. Белки - это..: а) полисахариды, б) полипептиды, в) полинуклеотиды. | 2. Биологические свойства белка определяет структура: а) третичная, б) вторичная, в) первичная. |
| 3. Первичная структура белка поддерживается за счёт связей: | 3. Вторичная структура белка поддерживается за счёт связей: а) ионных, б) пептидных, в) водородных. |
| 4. Гидролиз белка используется для: а) получения аминокислот, б) качественного обнаружения белка, в) разрушения третичной структуры | 4. Белки подвергаются реакциям: а) денатурации, б) полимеризации, в) поликонденсации. |
| 5. Аминокислоты, необходимые для построения белков, попадают в организм: а) с водой, б) с пищей, в) с воздухом. | 5. Какой из процессов наиболее сложен: а) микробиологический синтез, б) органический синтез, в) переработка растительного белка. |
Ответы: 1 - в, 2 - б, 3 - б, 4 - а, 5 - б. Ответ: 1 - б, 2 - в, 3 - в. 4 - а, 5 - б.
Тест «Белки»
1 . Какие химические элементы входят в состав белков?
а) углерод б) водород в) кислород г) сера д) фосфор е) азот ё) железо ж) хлор
2 . Сколько аминокислот участвуют в образовании белков?
а) 30 в) 20 б) 26 г) 10
3 . Сколько аминокислот являются незаменимыми для человека?
а) 16 б) 10 в) 20 г) 7
4 . В результате какой реакции образуется пептидная связь?
а) реакция гидролиза в) реакция поликонденсации
б) реакция гидратации г) все вышеперечисленные реакции
5 . Какая функциональная группа придает аминокислоте - кислотные, какая - щелочные свойства? (карбоксильная, аминогруппа).
6 . Какие связи образуют 1- первичную, 2- вторичную, 3- третичную структуры белка? Соотнесите:
а) ковалентные в) ионные
б) водородные г) такие связи отсутствуют
7 ) Определите структуры белковой молекулы:
1.  2.
2.

Таблица ответов
| Номер вопроса | |||||||
| Вариант ответа |
8) Денатурация - это разрушение белка до _____________структуры под действием________________, а также под действием растворов различных химических веществ (______,________, солей) и радиации.
9) Гидролиз - это разрушение _____________структуры белка под действием________________, а так же водных растворов кислот или щелочей.
10) Качественные реакции:
а) Биуретовая.
Белок + ___________________________ = _________________________
б) Ксантопротеиновая.
Белок + ___________________________ = __________________________
11) Установите соответствие между белками и их функцией в организме. Ответ дайте в виде последовательности цифр, соответствующих буквам по алфавиту:
БЕЛКИ: ФУНКЦИЯ:
А) гемоглобин 1)сигнальная
Б) ферменты 2) транспортная
В) антитела и антитоксины 3) структурная
4) каталитическая
5) защитная
12) Заполните значение белков:
| Функции | Значение |
|
| Строительная | Клеточные мембраны, покровные ткани, шерсть, перья, гора, волосы, хрящи |
|
| Транспортная | Накопление и транспорт по организму важнейших веществ |
|
| Энергетическая | Запас аминокислот для развития организма |
|
| Двигательная | Сократительные белки основа мышечных тканей |
|
| Защитная | Белки - антитела, антитоксины распознают и уничтожают бактерии и “чужеродные” вещества |
|
| Каталитическая | Белки - природные катализаторы (ферменты) |
|
| Сигнальная | Мембранные белки воспринимают внешние воздействия и передают сигнал о них внутрь клетки |
Вопросы к брифингу:
Белок иначе называют…
Что является мономерами белка?
Сколько незаменимых АК известно?
Каков атомарный состав белков?
Какая связь поддерживает вторичную структуру?
Как называется связь, образующая ППЦ?
Вторичная структура белковой молекулы в пространстве напоминает…
За счет каких взаимодействий образуются третичная структура?
Почему белки относят к ВМС?
Что в переводе с греческого означает “протеин”?
Что такое “денатурация”?
Как называется процесс взаимодействия белков с Н2О?
Согласно новой рецензии, опубликованной на сайте Applied Physiology, Nutrition and Metabolism , важно не только количество потребляемого белка, но и его источник. Есть целых три причины заботиться об этом.
Прежде всего, любой источник белка, будь то курица или арахис, содержит разное количество аминокислот - строительного материала для белков. Из 20 возможных аминокислот девять просто необходимы организму. Эти аминокислоты вы можете получить только из пищи. Так что очень важно правильно , включив в него разные продукты, богатые белком.
Продукты животного происхождения (мясо, яйца, молочные продукты) включают все необходимые аминокислоты в том или ином количестве, но большинство продуктов растительного происхождения содержат только фракции девяти необходимых аминокислот.
«Это значит, что если вы решили получать белок только из орехов, то организм будет лишён важных аминокислот», - объясняет соавтор исследования Райавель Иланго (Rajavel Elango), специалист по питанию и метаболизму.
Когда вы получаете белок из продуктов растительного происхождения, важно правильно подобрать их разновидности и количество, чтобы получить полную дневную норму необходимых аминокислот.
Конечно, это не повод отказываться от своих пищевых предпочтений и получать белки только из , поедая их на завтрак, обед и ужин. Такой рацион, помимо белка, включает большое количество калорий, жира и холестерина, что негативно сказывается на вашей фигуре и здоровье в целом. И это вторая причина следить за тем, какие продукты вы выбираете для насыщения организма белком.
И, наконец, третья причина - самая важная. «Каждый продукт, который служит для вас источником белка, включает определённое количество витаминов и минералов, - утверждает Иланго. - Некоторые продукты богаты витамином B, другие - железом, в третьих вообще практически нет полезных веществ».
Ваш организм не сможет усвоить полученный белок с максимальной пользой при недостатке важных питательных веществ.
Хотите убедиться в том, что получаете белок из правильных продуктов? Вот несколько самых полезных источников белка.
Яйца
liz west/Flickr.com«Мало того, что в каждом яйце содержится по 6 г белка, это ещё и наиболее полезный белок», - утверждает Бонни Тауб-Дикс (Bonnie Taub-Dix), американский диетолог, блогер и автор книги «Прочитайте, прежде чем съесть».
Белок, получаемый из яиц, имеет самую высокую усвояемость и помогает формировать ткани организма. Кроме того, яйца богаты холином и витаминами B 12 и D - веществами, важными для поддержания общего уровня энергии и её запаса в клетках организма.
Несмотря на распространённое мнение о том, что холестерин из яиц негативно влияет на работу сердца, вследствие чего можно употреблять этот продукт не чаще 2–3 раз в неделю, учёные доказали обратное. По результатам исследования, опубликованного в British Medical Journal, было установлено, что одно яйцо в день не влияет на работу сердца и не увеличивает риск инсульта.
Творог
«В одной порции творога (150 г) содержится около 25 г белка и 18% дневной нормы кальция», - говорит диетолог Джим Уайт (Jim White). Кроме того, творог богат казеином, медленно усваиваемым белком, который блокирует чувство голода на несколько часов.
Курица
 James/Flickr.com
James/Flickr.com
Птица должна быть основой белковой диеты. Она содержит меньше насыщенных жиров, чем большинство других видов мяса, и около 40 г белка в одной грудке (20 г белка на 100 г мяса). Иланго советует делать выбор в пользу белого мяса так часто, как можете, чтобы потреблять меньше калорий.
Цельное зерно
Цельнозерновые продукты полезны для здоровья и включают в себя гораздо больше белка, чем продукты из обычной муки. Например, хлеб из пшеничной муки первого сорта содержит 7 г белка, а цельнозерновой хлеб - 9 г белка на 100 г продукта.
Что более важно, цельнозерновые продукты обеспечивают организм клетчаткой, полезны для сердца и помогают контролировать вес.
Рыба
 James Bowe/Flickr.com
James Bowe/Flickr.com
«Рыба с низким содержанием калорий и множеством питательных веществ - это отличный источник жирных кислот омега-3, которые обеспечивают здоровье сердца и стабилизируют настроение», - утверждает Тауб-Дикс.
Среди самых полезных рыб - лосось и тунец. В одной порции лосося содержится около 20 г белка и 6,5 г ненасыщенных жирных кислот. А тунец - это настоящий кладезь белка: 25 г на 100 г продукта.
Если вы хотите избавиться от лишнего жира в организме, также стоит включить в свой рацион блюда из лосося: он содержит только 10–12 г жиров, насыщенных и ненасыщенных. Диетологи советуют есть рыбу дважды в неделю в запечённом или жареном виде.
Бобовые
 cookbookman17/Flickr.com
cookbookman17/Flickr.com
Греческий (фильтрованный) йогурт
Греческий йогурт может послужить завтраком, лёгкой закуской или ингредиентом для разных блюд. По сравнению с обычным йогуртом, в греческом почти в два раза больше белка: вместо 5–10 г в одной порции йогурта - 13–20 г. Кроме того, в греческом йогурте довольно много кальция: 20% от дневной нормы.
Орехи
 Adam Wyles/Flickr.com
Adam Wyles/Flickr.com
Орехи известны как продукт, богатый полезными ненасыщенными жирными кислотами, однако в них также содержится много белка. Кроме того, как показало исследование, опубликованное в 2013 году в New England Journal of Medicine, люди, съедающие горсть орехов в день, на 20% меньше подвержены риску смерти от разных недугов.
Зелень
 Jason Bachman/Flickr.com
Jason Bachman/Flickr.com
Разные виды зелени и зелёных листовых овощей богаты белком. Например, в 100 г шпината содержится всего 22 ккал и около 3 г белка, а в петрушке - 47 ккал и 3,7 г белка. Несмотря на то что в зелени недостаточно необходимых аминокислот, вы можете комбинировать её с бобовыми и получать достаточно белка и полезных веществ.
А какие продукты, богатые белком, предпочитаете вы?